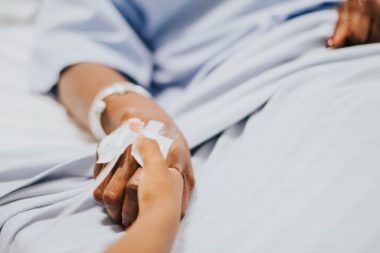
Datos de laboratorio recientes sugieren que el fármaco conserva su eficacia contra la variante ómicron de rápida propagación del coronavirus.
elfinanciero.com.mx
La píldora contra el COVID-19 de Pfizer mostró una eficacia cercana al 90 por ciento en la prevención de hospitalizaciones y muertes en pacientes de alto riesgo en un análisis final, informó este martes la farmacéutica estadounidense.
Mediante un comunicado, la empresa -que también es la creadora de una de las vacunas más empleadas contra el nuevo coronavirus- indicó que, además, sus datos más recientes confirman que el medicamento es un “inhibidor potente” ante la variante ómicron del COVID.
Pfizer dijo que el medicamento oral tenía una eficacia de alrededor del 89 por ciento en la prevención de hospitalizaciones o muertes en comparación con el placebo según los resultados provisionales en alrededor de mil 200 personas. Los datos divulgados este martes incluyen a mil personas más.
La farmacéutica aseguró que las personas que participaron en el ensayo y que recibieron el tratamiento de la píldora de Pfizer ninguna murió, en comparación con 12 muertes entre los que recibieron placebo.
Las píldoras de Pfizer, denominadas, Paxlovid, se toman con el antiviral ritonavir más antiguo cada 12 horas durante cinco días, comenzando poco después de la aparición de los síntomas.
Las píldoras aún no han sido aprobadas por la Administración de Fármacos y Alimentos (FDA, por sus siglas en inglés) de Estados Unidos, pero el director ejecutivo de Pfizer, Albert Bourla, se mostró esperanzado a principios de diciembre de que se pueda recibir el visto bueno antes de que concluya el año.
En los estudios clínicos, la reducción del riesgo de hospitalización o muerte por COVID-19 fue del 89 por ciento cuando la pastilla se administró en los tres días siguientes a la aparición de los primeros síntomas; y prácticamente la misma (del 88 por ciento) cuando se administró en los cinco días posteriores a la aparición de síntomas, informó la farmacéutica.
El estudio de Pfizer se llevó a cabo entre 2 mil 246 adultos residentes en Norte y Sudamérica, Europa, África y Asia (41 por ciento de ellos en EU) a los que se les había diagnosticado COVID-19 en los cinco días anteriores, y todos ellos tenían por lo menos una característica o condición médica que les hacía ser pacientes con riesgo de desarrollar una enfermedad grave.